電子移動・励起移動
「光合成装置が光エネルギーを“捨てる”謎を解く」
■背景
光合成の反応は光エネルギーでクロロフィル色素から電子を引き抜く反応(電荷分離)で開始されます(参考文献1)。この反応を駆動するのは「光合成装置」と称される色素のタンパク質の超分子複合体です。光合成装置は、100%に近い効率で吸収した太陽光をクロロフィルの電荷分離に繋げる能力を秘めていますが、環境中では集めた光エネルギーの一部を積極的に捨ててしまいます(図1)。これは「非光化学的消光」と呼ばれる現象で、生物の光合成の処理能力を超えるほどの“強すぎる光”から光合成装置や細胞を守るためにあると考えられています。しかし、その詳細な反応機構や進化的な成立過程はまだ謎に包まれています。
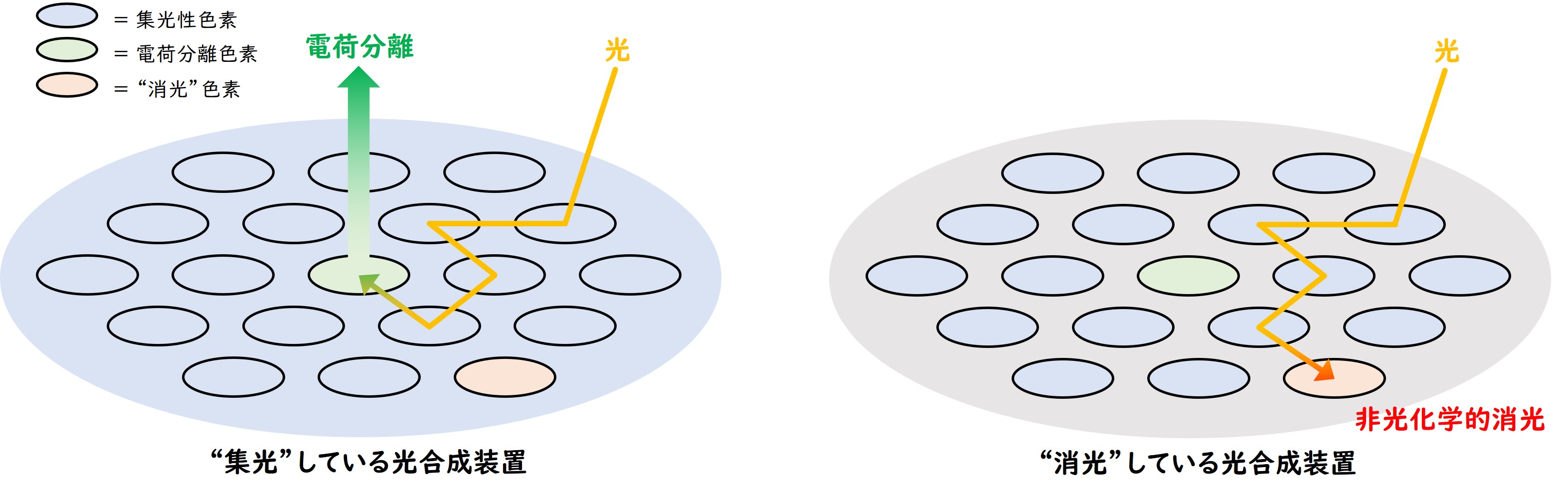
図1 光合成装置で起こる非光化学的消光の概念図。光合成装置にはたくさんの色素分子が結合しており、実際に光合成の反応を駆動しているのは特別な“電荷分離色素”だけである。たいていの場合、その他の多数の“集光性色素”のどれか1分子が光を吸収する。その光エネルギーが電荷分離色素まで伝達されると電荷分離が起こり、光合成の反応が開始される(左図)。光エネルギーが“消光色素”に伝達されると、非光化学的消光によって光エネルギーは光合成に使われずに散逸する。
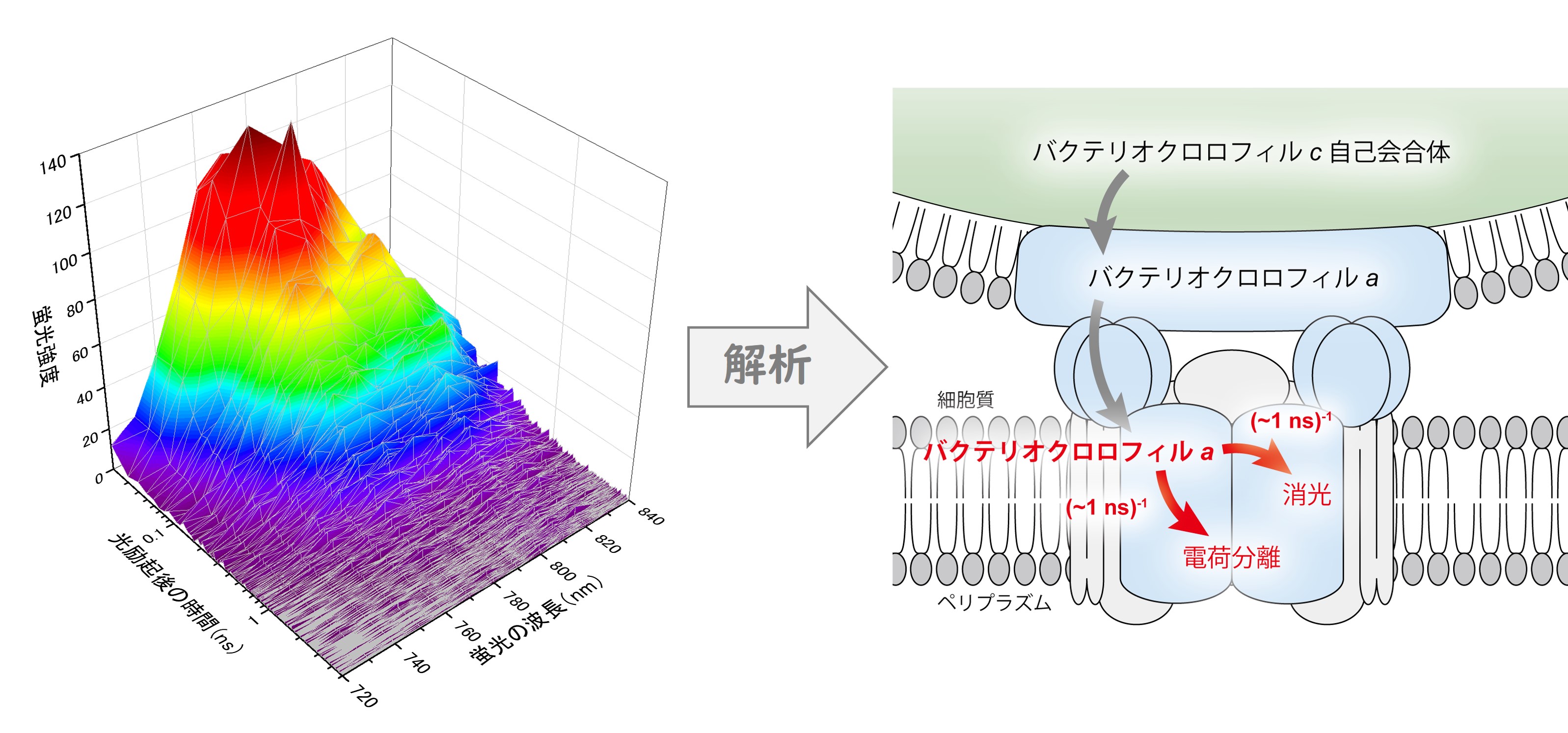
図2 緑色硫黄細菌で発見された嫌気的な非光化学的消光(参考文献3)。緑色硫黄細菌の細胞の時間分解蛍光スペクトル(左図)を解析した結果、光合成装置のなかで起こるエネルギー伝達系の最終段階で恒常的な消光が起こっていることがわかった(右図)。
■研究概要
非光化学的消光は、光を吸収したクロロフィルからカロテノイドへエネルギーが伝達されることで起こると考えられています。カロテノイドには光を捨てる機能だけでなく、逆に光を集めてクロロフィルに伝達する機能もあるため、非光化学的消光を駆動する色素分子を光合成装置の中から探し出す必要があります(例えば、図1の「消光色素」)。たくさんの色素分子のうち、どの色素からどの色素にエネルギーが伝達され、どのように光を捨てているのかを解明する研究が、様々な生物の光合成装置で進められています。
非光化学的消光の研究から、既知の光合成の理解に見直しを迫るような成果も報告されています。これまでの理解では、光合成生物に対する“強すぎる光”の悪影響は高い細胞毒性をもつ活性酸素種の生成に依るものと考えられてきました。しかし、緑色硫黄細菌という全く酸素の無い環境でしか光合成しない生物(参考文献2)でも非光化学的消光は起こっていることが分かりました(図2;参考文献3)。非光化学的消光は活性酸素種に対する防御以外にも重要な役割をもつことが考えられます。また非光化学的消光は地球上に酸素が溢れる以前から存在し、進化的に非常に古い起源をもつことも意味しています。
■科学的・社会的意義
非光化学的消光は天然の光合成に特徴的な現象です。様々な分野で「人工光合成」の実現を目指した研究が進められていますが、天然の光合成が非光化学的消光によって敢えて反応効率を落とす理由はわかっていません。非光化学的消光を駆動する具体的な分子種やタンパク質の構造、また詳細な反応機構の理解が進むことで、天然の光合成の高い効率と堅牢性の解明に繋がり、延いては人工光合成への応用が期待されます。
■参考文献
1)杉浦美羽、伊藤繁、南後守 編 「光合成のエネルギー変換と物質変換―人工光合成を目指して」 化学同人
2)嶋田敬三、高市真一 編 「光合成細菌―酸素を出さない光合成」 裳華房
3)C. Azai et al. (2020) “Anaerobic energy dissipation by glycosylated carotenoids in the green sulfur bacterium Chlorobaculum tepidum.” J. Photochem. Photobiol. A 403:11282
■良く使用する材料・機器
1) 紫外可視分光光度計(島津製作所)
2) 分光蛍光光度計(堀場製作所、日立ハイテクサイエンス)
3) 高速液体クロマトグラフ(島津製作所)
4) 嫌気グローブボックス(米国Coy社)
5) 実験試薬(和光純薬株式会社、ナカライテスク)
 2022年分野別専門委員
2022年分野別専門委員
立命館大学・生命科学部
浅井智広 (あざいちひろ)
https://research-db.ritsumei.ac.jp/rithp/k03/resid/S001053
「光合成タンパク質内の励起移動・電子移動反応を理論的に解明」
■背景
光合成反応は、光エネルギーを用いて水分子から水素を取り出し、大気中の二酸化炭素と結合することにより、炭水化物を作り出す反応である。この反応は光合成生物の細胞内に共存している葉緑体内で起こる。特に初期反応は二段階あり、光エネルギーを捕獲して集める“励起移動”、次に、集めたエネルギーから電子を分離させて移動する“電子移動”という反応がある。これらは、光捕集系(内部にクロロフィル、カロテノイド等の色素分子が存在する)と、反応中心(クロロフィル二量体(スペシャルペア)、フェオフィチン、キノンが存在する)というタンパク質中で起こる(図1)。本研究は、これら2種類の反応に関わる時間及び空間の情報(速度と経路)を調べ、実験と比較することによって光合成初期反応に関わる機能の本質の理解を深めることを目的とする。
タンパク質は高分子の一つであり、その構成要素は、水素、炭素、窒素、酸素等の原子からなる。各原子は原子核と電子から構成されている。生物物理学におけるタンパク質の機能解明に関わる研究では、主にこのスケールの粒子を最小単位としている。これを基に、反応を引き起こす際に発生する力の源となる相互作用エネルギーの大小関係が、反応メカニズムとどのように関わっているかを調べることが基礎的な研究である。
色素間の励起移動相互作用Uが、励起状態-原子核間の相互作用λに比べて非常に大きな極限(U >>λ)の場合、励起エネルギーは対象としている系全体に非局在化した電子励起状態を形成する。逆の極限(U <<λ)の場合は、励起エネルギーは系のどこかに局在化する。このような両極限に対応した場合の反応を記述する理論は既に構築されている。ところが、光捕集系内の各色素の配置は、Uとλが同程度(U~λ)の中間結合的な場合があり、光捕集を行う際に「生体系はこの環境下でどのように反応を引き起こしているのか?」という疑問がある。このことを明らかにするためには、量子力学、統計力学を駆使し、反応が行われる際に、速度や経路などのメカニズムを解析するための、一般的な理論的枠組みを再構築する必要がある。
■研究概要
【中間結合励起移動理論】
中間結合的な環境下での励起移動が行われる場合、現象として本質的に重要なメカニズムは一体何なのか?を理解する必要がある。その為に我々は、Uの大きさがλに比べて非常に大きい極限と、小さい極限での励起移動理論を説明出来る統一理論の構築を試み、中間結合領域での励起移動メカニズムを分類することができる公式の導出を行った(文献[1]、図2)。
様々な光捕集系内の色素分子の数は複数個存在し、一見すると乱雑に配置されている。そのため、上記基礎理論構築の研究と共に、これらの色素が配置されている場合の励起移動メカニズムを理解するために必要な理論構築を行っている。その第一段階として、二つの色素間(ドナー、アクセプター)の励起移動を考察する際、その他の色素(メディエイター)が存在することにより生じる励起移動メカニズムの影響を調べるための基礎理論の構築を行った。メディエイターを考慮していない場合に比べ、メディエイターの相対的な配置、及び、その電子励起状態等により、移動速度が大きく変動すること、また、その一般的な性質を明らかにした(文献[2]、図3)。
【光捕集系2(LH2)】
1995年に光合成バクテリアが持っている光捕集系2(LH2)のX線結晶構造解析が行われ、高分解能の3次元構造が明らかとなった。その3次元構造は非常に高い回転対称性を持ったリング状であり、その中の色素は、粗に配置されている色素集団が800nmの光を吸収するB800と、密に配置されている色素集団が850nmの光を吸収するB850から構成されている。
B800からB850への励起移動は約1psの移動時間という超高速現象であることが実験的に観測されている。この実験結果を従来の理論(フェルスター理論)によって見積もると、1万倍ほど遅くなってしまうという問題が生じた。当時、この問題を理論的に改善することは困難であることが解ってきた。そのため、フェルスター理論の改良が多くの理論研究者によって精力的に行われた。
一方、光捕集系2(LH2)内のB800色素を置換し、移動速度を観測する実験が行われた。しかし、当時報告されている最新理論を基にした解析結果は、実験結果を十分に再現することが出来たとは言い難い。筆者はこの問題を、一般化マスター方程式と呼ばれる方程式を用いて理論的解析を行い、実験結果を定量的に再現することに成功した。(図5)この結果として以下のことを仮説として提案している。光捕集系内の励起移動機構では、系の原子核の揺らぎ方に応じて励起状態の量子的波動性が、空間的に広がった“非局在励起子”を形成しようとする過程と、部分的に捕らわれた“局在励起子”を形成しようとする過程、の二つが拮抗しながら起こる場合がある。(文献[3])
【電子移動】
電子移動反応は、生体反応から電子デバイスに至るまで、反応の素過程の一つとして重要な役割を果たす。電子移動反応では、以下の二つのプロセスが重要である。
①反応を引き起こす為に必要な原子配置が、反応前後のエネルギーが保存した遷移状態へと分子環境の熱揺らぎを通して到達する。
②上記の原子配置の状況で、電子が量子力学的トンネル効果によって遷移する。
1990年代後半の頃までの理論解析では、X線結晶構造や分子力学法最適化構造などの全原子が固定された一点構造を基にして量子化学計算を実行し、そして、マーカスの速度式中の重要なパラメータである電子因子(②の量子力学的トンネル効果で電子が遷移するために必要な相互作用エネルギー)を求めていた。ところが、それ以後の計算機能力の著しい進歩によって、電子移動反応を引き起こすタンパク質系に分子動力学シミュレーションを適用し、得られる各構造全てに量子化学計算を行うことが可能となってきた。西岡らは、原子核の熱運動の効果を取り入れた電子因子を解析した結果、フェムト秒(10の-15乗秒)の時間スケールで複雑に揺らいでいることを明らかにした。
このことは、電子因子に対して従来適用してきたコンドン近似という仮定(電子遷移の相互作用エネルギーの大きさが、原子核の座標に殆ど依存しない)を破る発見である。そこで、非コンドン電子移動速度理論が構築された。この理論を基に、コンドン近似の破れが電子移動速度のエネルギーギャップ(反応前と反応後のエネルギー差ΔG)依存性に及ぼす影響について調べた。その結果、Ru-modifiedチトクロームCタンパク質中電子移動 に関する逆転領域(-ΔG >λ)での速度依存性を定性的に説明できる理論的枠組みであることが明らかとなった。すなわち、光合成に関わるタンパク質中電子トンネル移動反応では、状態②の電子トンネル移動において、遷移前後のエネルギー保存則を保ちつつ、その量子力学的中間状態において電子-核間の衝突によるエネルギーの交換が起こりうる(非弾性散乱電子移動反応)ことを示している。(文献[4,5]、図6)
■科学的・社会的意義 地球上の生命体の多くが生きるために必要なエネルギーの殆どは、太陽から放射され地上に降り注ぐ光エネルギーが起源となっている。このエネルギーの獲得を可能にした反応が光合成である。一方、地球誕生後に大気中の酸素濃度が高くなった結果、呼吸反応によるエネルギーの獲得が可能となるように多くの生物は進化してきた。地球上のあらゆる生命体は光合成生物と呼吸反応を利用した生物からなっており共存関係にある。本研究に限らず、多くの研究者によって、光合成反応の理解は深まりつつある。著者は励起移動と電子移動の反応に関する理論研究に携わっている。本研究は、膨大な年月をかけて自然の中で生み出された、エネルギーを獲得する仕組みの偉大さをより深く認識するための一助となる、と願っている。
■参考文献
[1] Advanced Theory of Excitation Energy Transfer in Dimers , A. Kimura and T. Kakitani , J. Phys. Chem. A , 111巻 (頁:12042) , 2007年
[2] General theory of excitation energy transfer in donor-mediator-acceptor systems , Akihiro Kimura , The Journal of Chemical Physics , 130巻 (頁:154103) , 2009年
[3] Theoretical Analysis of the Energy Gap Dependence of the Reconstituted B800 f B850 Excitation Energy Transfer Rate in Bacterial LH2 Complexes , A. Kimura and T. Kakitani, J. Phys. Chem. B, 107巻(頁:7932), 2003年
[4] Interference, Fluctuation, and Alternation of Electron Tunneling in Protein Media 1. Two Tunneling Routes in Photosynthetic Reaction Center Alternate Due to Thermal Fluctuation of Protein Conformation. , H. Nishioka, A. Kimura, T. Yamato, T. Kawatsu, T. Kakitani , J. Phys. Chem. B , 109巻 (頁:1978) , 2005年
[5] Interference, Fluctuation, and Alternation of Electron Tunneling in Protein Media. 2. Non-Condon Theory for the Energy Gap Dependence of Electron Transfer Rate. , H. Nishioka, A. Kimura, T. Yamato, T. Kawatsu T. Kakitani , J. Phys. Chem. B , 109巻 (頁:15621) , 2005年
■良く使用する材料・機器 Linux搭載DOS/V計算機、
■図一覧
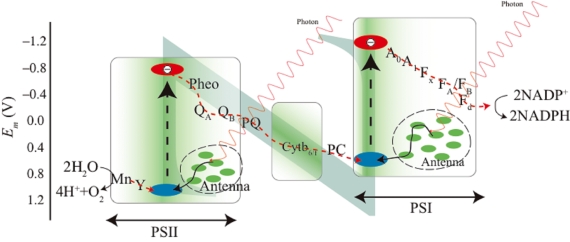
図1:光合成初期反応を示すZスキーム。Antenna中の黒曲線が励起移動。赤ダッシュ曲線が電子移動を表す
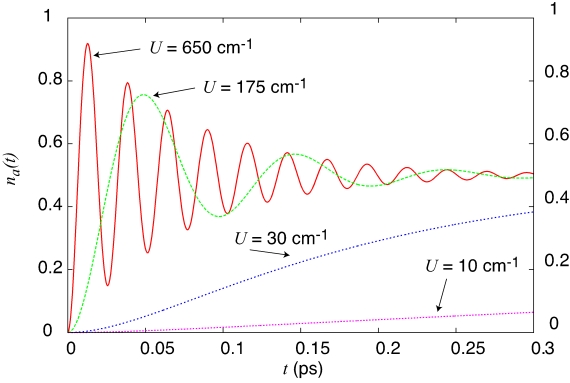
図2:二量体内中間結合励起移動。横軸は時間、縦軸はアクセプター分子が励起状態である確率をあらわす。相互作用エネルギーUが、ある境界値よりも大きくなると振動の性質が表れ、小さい場合は単調増加の性質を持つことを示す。
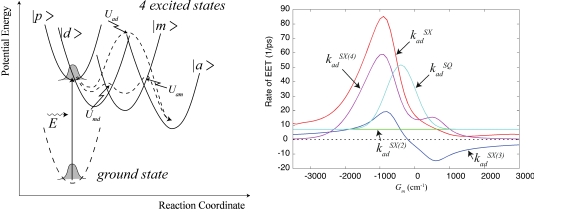
図3:(左図)三つの色素分子系から構成される励起移動のモデル。それぞれ、p:ドナー分子を光エネルギーEにより励起させた直後、d:ドナー分子が励起状態、m:メディエイター分子励起状態、a:アクセプターが分子励起状態、を表す。(右図)メディエイターが速度にどのような影響を与えるかを示す。横軸はドナー、アクセプター分子の励起エネルギーを基準としたメディエイターの励起エネルギーである。
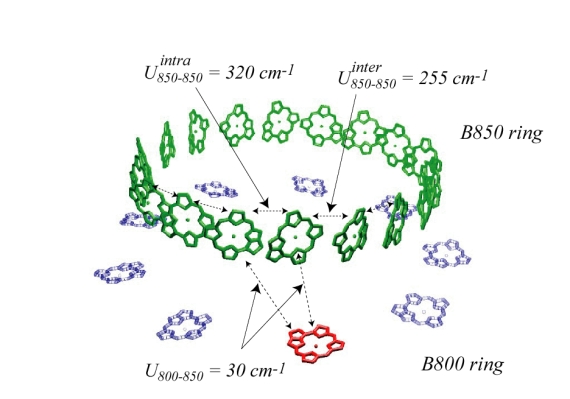
図4: LH2の3次元構造。図で表されている分子は全てバクテリオクロロフィル(BChl)である。緑色で表したBChlの集団がB850、それ以外のBChlがB800である。
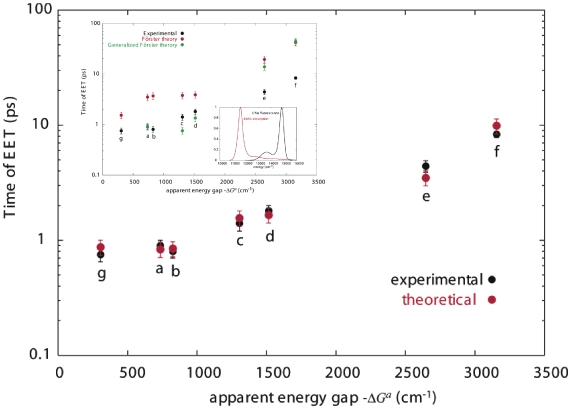
図5:LH2内のB800を色素置換した場合の、色素置換したB800からB850へ励起移動の移動時間に関する、実験(黒)と理論(赤)の比較。
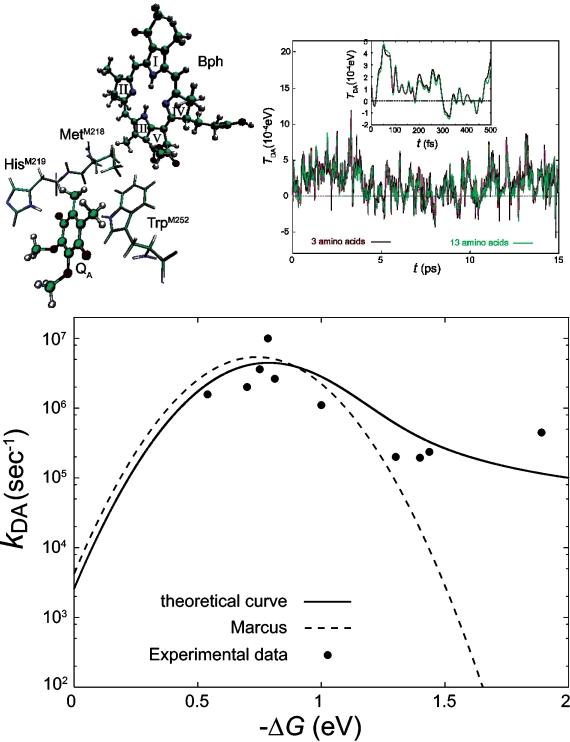
図6:光合成バクテリア反応中心内のバクテリオフェオフィチンとキノンA間の電子移動系(左上図)と、その電子トンネル行列要素の時間変化(右上図)。Ru-modifiedチトクロームCタンパク質中電子移動速度に関するエネルギーギャップ依存性の実験結果と非弾性散乱電子移動理論を比較したグラフ(下図)。
 H24年度分野別専門委員
H24年度分野別専門委員
名古屋大学大学院理学研究科
木村明洋 (きむらあきひろ)
https://www.tb.phys.nagoya-u.ac.jp/~akimura/
