情報伝達分子
「フラビン結合型光センサータンパク質の反応機構」
■背景
生物は外界の光を情報やエネルギー源として利用するために、光を吸収する色素(発色団)を結合したタンパク質を用いています。我々ヒトを含む動物の視覚を司るタンパク「ロドプシン(色素はレチナール)」や植物の光合成の「光化学系複合体(色素はクロロフィルやカロテノイド)がタンパク質機能しています。
光を情報として利用することは動物だけでなく植物やある種の細菌も行っています。その中で、1990年代半ばから2000年代初めにかけてフラビンを発色団とする光センサータンパク質の発見が報告されてきました。フラビンはビタミンB2誘導体であり、光センサータンパク質の色素として利用される前から、呼吸の電子伝達などに関わる補酵素として知られていました。
興味深いことに、光センサーとして機能するフラビンタンパク質でありながらその光反応が異なる複数種類のタンパク質が存在します(図1)。同じ色素であるにも関わらず、何故異なる光反応を示すのでしょうか?フラビンを取り囲んでいるタンパク質環境(アミノ酸残基)がそれらの反応性を決めているとすれば、それを決定するものは何でしょうか?
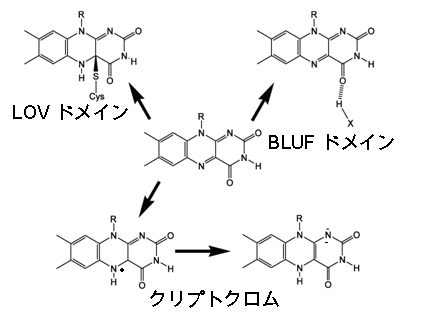
図1 フラビンタンパク質の異なる光反応。
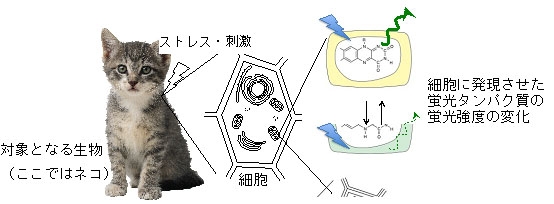
図2 細胞内の酸化還元状態に応答して蛍光強度を変化させる蛍光タンパク質の開発。
■研究概要
私は何故フラビンタンパク質の光反応が異なるのかという点に興味を持ち、フラビンの光反応を制御するタンパク質環境の要因を決定することを研究目的とします。紫外・可視、蛍光、及び赤外の各分光法を用いることにより、光反応機構や反応後のタンパク質構造変化について解析を行うことを考えています。
またこれらの光反応機構を理解することで、応用研究として、フラビンタンパク質の蛍光性を利用した細胞内の環境に応答した蛍光タンパク質の作製(図2)を行っています。
■科学的・社会的意義 光反応機構を知ることが出来れば、光センサーデバイスとしての応用が期待されます。また、環境応答性蛍光タンパク質の開発によって、細胞内の環境について細胞を破壊することなく情報を得ることが出来るようになります。
■参考文献
1)Iwata, T., Watanabe, A., Iseki, M., Watanabe, M. and Kandori, H. (2011) "Strong Donation of the Hydrogen Bond of Tyrosine during Photoactivation of the BLUF Domain", J. Phys. Chem. Lett. 2, 1015-1019.
2)Iwata, T., Tokutomi, S. and Kandori, H. (2011) "Light-induced structural changes of the LOV2 domains in various phototropins revealed by FTIR spectroscopy" BIOPHYSYCS 7, 89-98.
■良く使用する材料・機器
1) 紫外・可視分光光度計(日本分光株式会社・株式会社島津製作所)
2) フーリエ変換赤外(FTIR)分光光度計(アジレント・テクノロジー)
3) 蛍光分光光度計(日本分光株式会社)
4) 実験試薬(和光純薬株式会社)
H24年度分野別専門委員
名古屋工業大学・若手研究イノベータ養成センター
岩田達也(いわたたつや)
